Antybiotyki ostatniej szansy pod lupą
Badaczki z Uniwersytetu Warmińsko-Mazurskiego w Olsztynie analizują obecność bakterii antybiotykoopornych w ściekach szpitalnych. O pierwszych wynikach projektu – i o tym, co mówią one o skali problemu – opowiadają prof. dr hab. inż. Ewa Korzeniewska i prof. dr hab. inż. Monika Harnisz w rozmowie z Lidią Sulikowską.



Fot. magnific.com, arch. prywatne
Jaki jest mechanizm narastania zjawiska antybiotykooporności?
Monika Harnisz: Oporność drobnoustrojów na antybiotyki rozprzestrzenia się głównie przez wymianę nabytych mechanizmów oporności na dany lek, które są kodowane w DNA bakterii. Dochodzi do tego w tzw. procesie horyzontalnego transferu genów, który najczęściej polega na wymianie plazmidowego DNA pomiędzy bakteriami. Niektóre bakterie mają bardzo plastyczne genomy, które łatwo poddają się temu procesowi. Wymianie sprzyja obecność antybiotyków w środowisku – zarówno w ciele ludzkim, jak i zwierzęcym, ale też w glebie, wodzie czy ściekach, czyli wszędzie tam, gdzie występuje duże zagęszczenie bakterii.
Rachunek jest prosty: im więcej spożywamy antybiotyków, tym bakterie mają większe szanse na nabywanie mechanizmów oporności, a następnie ich transfer. To nie jest jedyny problem. Pacjenci często nie mają świadomości, że przerywając kurację antybiotykową wcześniej, niż zalecił lekarz, także przyczyniają się do powstawania lekooporności, bo przecież niedoleczona infekcja może prowadzić do mnożenia się w organizmie opornych bakterii. Innym problemem jest wyrzucanie antybiotyków do kosza ze zwykłymi odpadami zamiast do przygotowanych do tego pojemników w aptekach. To powoduje, że leki nie trafiają do specjalnej utylizacji, ale na zwyczajne wysypisko śmieci, skąd przedostają się do wody i gleby. Wydaje mi się jednak, że świadomość w tym zakresie wzrasta.
Ewa Korzeniewska: Horyzontalny transfer genów pomiędzy bakteriami umożliwia rozprzestrzenianie się lekooporności pomiędzy krajami na całym świecie, bo przecież często podróżujemy. Dlatego tak ważne jest wdrażanie działań hamujących to zjawisko ponad granicami państw.
Z którymi lekami jest największy problem?
E.K.: Na świecie bardzo dużo zużywa się antybiotyków beta-laktamowych, co przekłada się na wzrost oporności bakterii, przeciwko którym są one stosowane. Na szczególną uwagę zasługują drobnoustroje zdolne do produkcji enzymów ESBL, które nadają oporność na wiele powszechnie stosowanych antybiotyków, w tym penicyliny, cefalosporyny oraz monobaktamy. To patogeny alarmowe, do których zaliczamy m.in. bakterie rzędu Enterobacterales, w tym Escherichia coli i Klebsiella pneumoniae. Są one coraz bardziej oporne na cefalosporyny 3. generacji oraz karbapenemy.
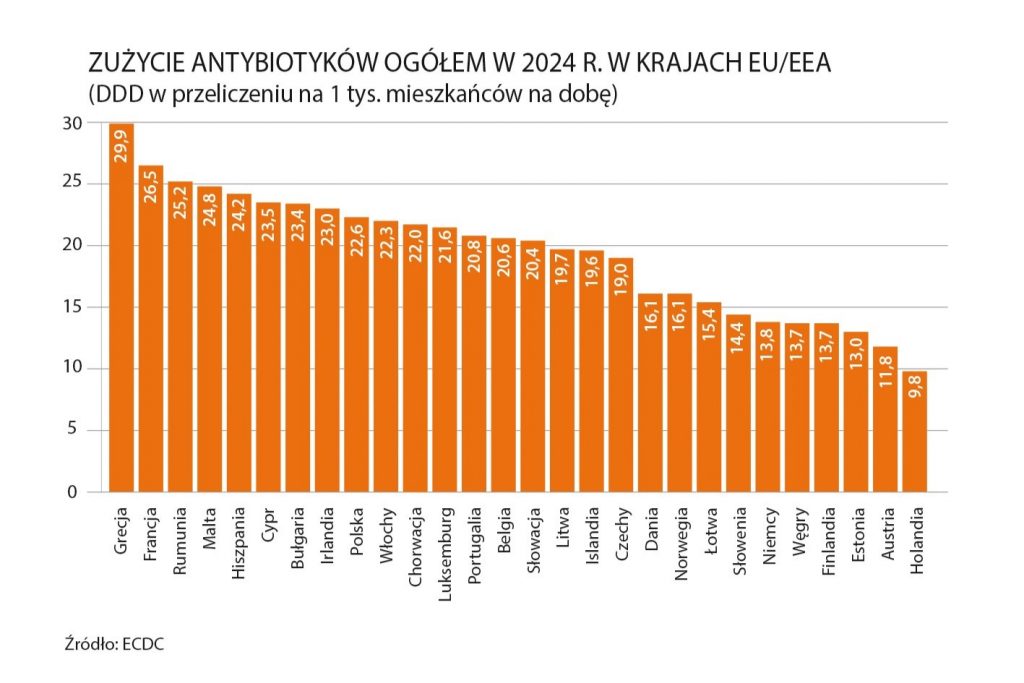
Jak dużo antybiotyków zużywamy w Polsce?
E.K.: W dalszym ciągu zbyt dużo, ale na szczęście obserwujemy poprawę. Z opublikowanego kilka miesięcy temu raportu Europejskiego Centrum ds. Zapobiegania i Kontroli Chorób (ECDC) wynika, że w spożyciu antybiotyków ogółem, czyli zarówno tych podawanych w szpitalach, jak i ordynowanych w lecznictwie ambulatoryjnym, zajmujemy 9. Miejsce w Unii Europejskiej. To najnowsza analiza tej organizacji, zawierająca dane za 2024 r. Pięć lat temu byliśmy na 6. pozycji, więc jest lepiej, ale nadal mamy sporo do zrobienia. Średnia UE/EEA w spożyciu antybiotyków wyniosła 20,2 definiowanej dawki dobowej (DDD, ang. Daily Defined Dose) w przeliczeniu na 1000 mieszkańców na dobę. W Polsce osiągnęliśmy poziom 22,6, ale np. Holandia uzyskała wynik poniżej 10. Niechlubnymi liderami rankingu są Grecja (29,9), a za nią Francja (26,5), Rumunia (25,2), Malta (24,8) i Hiszpania (24,2).
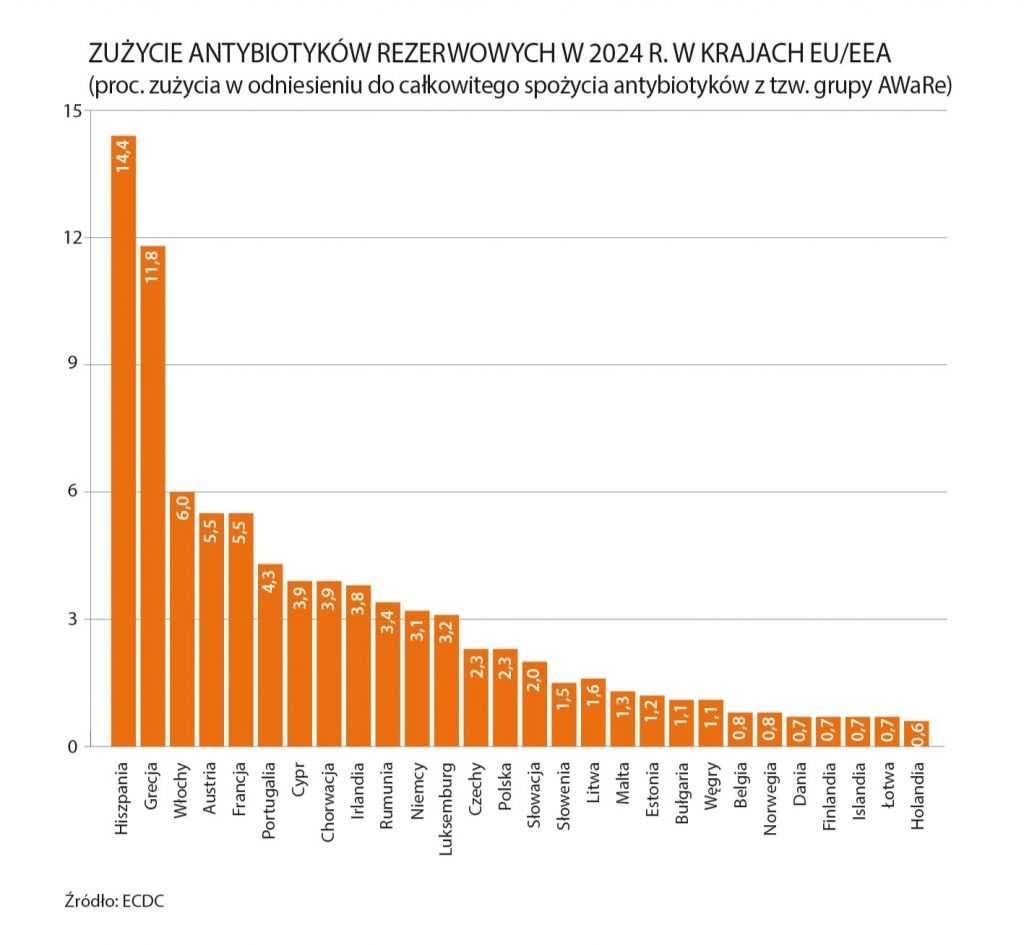
A w przypadku wyłącznie antybiotyków rezerwowych, czyli leków ostatniej szansy stosowanych w warunkach szpitalnych?
E.K.: Akurat w tym aspekcie wypadamy nieźle na tle Europy, ale nie jest tak dobrze, jakby mogło się na pierwszy rzut oka wydawać. Najnowszy raport ECDC pokazuje, że średnia UE/EEA dotycząca zużycia antybiotyków rezerwowych, uznanych przez WHO jako leki, które powinny być stosowane w ostateczności, wyniosła 5,4 proc. w odniesieniu do całkowitego spożycia antybiotyków zaliczanych do grupy AWaRe, czyli opracowanej przez WHO w 2017 r. klasyfikacji wspierającej zarządzanie antybiotykami. Te dane należy jednak rozpatrywać w szerszym kontekście, ponieważ są ogromne różnice między krajami. Średnia jest mocno zawyżona przez Hiszpanię (14,4 proc.) i Grecję (11,8 proc.). Siedem krajów, w tym Finlandia i Belgia, uzyskały wynik poniżej 1 proc., a kolejnych siedem państw było w przedziale 1–2 proc. Polska osiągnęła wynik 2,3 proc., więc zdecydowanie poniżej średniej, ale uwaga – jeszcze w 2020 r. spożycie antybiotyków rezerwowych w naszym kraju było na poziomie 1,3 proc., co oznacza, że mamy tendencję wzrostową, i to znaczną. W mojej ocenie jest to związane z tym, że przez długi czas te leki były bardzo drogie, więc szpitale bardziej ograniczały ich zużycie.
Wspólnie z badaczkami z Politechniki Śląskiej badają Panie częstość występowania w ściekach szpitalnych antybiotyków rezerwowych i bakterii, które są na nie oporne. Co konkretnie podlega tej analizie?
E.K.: Z realizacją projektu wystartowałyśmy dwa lata temu, po przyznaniu grantu Narodowego Centrum Nauki na ten cel. Zespół badaczek z Politechniki Śląskiej w Gliwicach pod kierunkiem prof. Sylwii Bajkacz z Katedry Chemii Nieorganicznej, Analitycznej i Elektrochemii na Wydziale Chemicznym PŚ analizuje próbki ścieków pod kątem zawartości antybiotyków rezerwowych, przede wszystkim karbapenemów, z kolei my bierzemy pod lupę obecność drobnoustrojów wykazujących oporność na te antybiotyki, głównie Enterobacterales, w tym Klebsiella pneumoniae, a także Pseudomonas aeruginosa i Acinetobacter baumannii. Dzięki temu zyskujemy pełny obraz tego, co znajduje się w ściekach szpitalnych.
Ile szpitali bierze udział w badaniu?
E.K.: Skontaktowałyśmy się z ponad 80 placówkami, z czego zdecydowana większość się zgodziła udostępnić nam próbki do badań. W projekcie bierze udział 3-5 szpitali z każdego województwa, zarówno dużych, jak i mniejszych, liczących od 100 do ponad 1000 łóżek. Jesteśmy na półmetku realizacji projektu. Zakończyłyśmy pobór próbek w terenie, mamy również za sobą mikrobiologiczne badania hodowlane. Co ważne, pobierałyśmy próbki ścieków zarówno w sezonie zimowym, jak i letnim. Z uwagi na znaczące różnice w spożyciu antybiotyków w tych okresach chciałyśmy sprawdzić, jak to się przekłada na obecność antybiotyków i bakterii lekoopornych.
Jest to przełożenie?
E.K.: Jesteśmy w trakcie szczegółowych analiz, ale statystycznie już widzimy taką zależność. Zresztą to niejedyna kwestia, którą porównujemy. Próbki analizowałyśmy również pod kątem zróżnicowania w zależności od wielkości szpitali, od regionu, bierzemy też pod uwagę czynniki socjoekonomiczne w danym regionie, spożycie antybiotyków w danym szpitalu, liczbę pacjentów leczonych antybiotykami etc.
Co już udało się ustalić?
M.H.: Myślałyśmy, że w ściekach szpitalnych nie będzie zbyt wiele drobnoustrojów lekoopornych. Wyniki bardzo nas zaskoczyły. Ze 150 próbek udało nam się wyizolować ponad 5000 szczepów karbapenemoopornych bakterii, a są to tylko wyniki z badań hodowlanych. Przed nami jeszcze analizy molekularne, dzięki którym poznamy odpowiedź, jaką pulę genów lekooporności niosą wszystkie mikroorganizmy zawarte w ściekach szpitalnych, zarówno żywe, jak i martwe czy hodowalne i niehodowalne, w stosunku do tych, które występują w innych krajach. Raczej nie spodziewamy się różnic, ale zobaczymy, co się okaże.
E.K.: W ściekach szpitalnych w całej Polsce znalazłyśmy bardzo dużo lekoopornych bakterii z rzędu Enterobacterales, z czego zdecydowanie najwięcej Klebsiella pneumoniae opornych na karbapenemy. Zidentyfikowaliśmy także m.in. bakterie Enterobacterales oporne na cefalosporyny, a także spory odsetek patogenów wielolekoopornych, i to nie tylko z tego rzędu, ale też Pseudomonas aeruginosa i Acinetobacter johnsonii, za to mniej liczne były karbapenemooporne Acinetobacter baumannii. W ściekach były też antybiotyki rezerwowe z grupy karbapenemów i inhibitory karbapenemów. Niedawno ukazała się praca jednej z doktorantek z zespołu prof. Bajkacz przedstawiająca dane na ten temat.
Czy wyniki różnią się pomiędzy szpitalami?
E.K.: W tym momencie mogę zdradzić, że zaobserwowałyśmy istotne różnice w częstości występowania lekoopornych bakterii pomiędzy regionami na południu Polski, które są bardzo zaludnione i rozwinięte gospodarczo, a północą naszego kraju, np. regionem Warmii i Mazur, gdzie gospodarka nie jest tak rozwinięta. Wykazałyśmy też, że różnice występują nie tylko między województwami, ale również pomiędzy poszczególnymi szpitalami. Udało się nam też powiązać występowanie karbapenemoopornych Klebsiella pneumoniae z czynnikami ekonomicznymi, np. ze stopą bezrobocia. Nie możemy jeszcze upubliczniać wszystkich ustaleń, bo są one wykorzystywane do prowadzonych doktoratów. Na koniec projektu planujemy zrobić stronę internetową z interaktywnymi mapami, które będą wskazywać wyniki ze wszystkich województw.
Jak bardzo częstość występowania bakterii lekoopornych w ściekach wynika ze zużycia antybiotyków rezerwowych w danym szpitalu?
E.K.: Dzięki temu, że szpitale udostępniły nam swoje dane dotyczące zużycia antybiotyków rezerwowych, mogłyśmy tę zależność zbadać. Tam, gdzie zużycie było większe, mamy w ściekach więcej antybiotyków i bakterii antybiotykoopornych.
Czy szpitale poznały swoje wyniki?
E.K.: Tak, na tym etapie każdy ze szpitali otrzymał raport, jak wypadł na tle województwa i całej Polski. Myślę, że to dla nich bardzo ciekawy materiał do analizy. Jesteśmy otwarte na dalsze pytania i współpracę.
M.H.: Dopowiem tylko, że próbki pobierałyśmy z takiego miejsca kanalizacji szpitalnej, które zbiera ścieki ze wszystkich oddziałów. To ścieki, które bezpośrednio są odprowadzane do kanalizacji miejskiej. Zależało nam na tym, aby zobaczyć, jaki ładunek tych zanieczyszczeń uchodzi do kanalizacji miejskiej i potem trafia do oczyszczalni ścieków, a stamtąd do środowiska naturalnego. Szpitale nie mają obowiązku posiadania własnej oczyszczalni ścieków, więc zazwyczaj ich nie mają, czemu trudno się dziwić, bo to kosztowna inwestycja. Wyjątek stanowią te placówki, które mają oddziały zakaźne. Ścieki z takich oddziałów muszą być dezynfekowane.
To, że ścieki szpitalne trafiają do kanalizacji miejskiej, może stanowić zagrożenie sanitarno-epidemiologiczne?
M.H.: Zdecydowana większość drobnoustrojów ginie na etapie oczyszczania ścieków, ale niektóre patogeny, w szczególności bakterie wielolekooporne mają dużą siłę przetrwania. Są mało wymagające, świetnie sobie radzą w kanalizacji, a stamtąd mogą trafiać do środowiska, przekazując oporność kolejnym bakteriom, żyjącym na przykład w wodach powierzchniowych. Od 2025 r. obowiązuje dyrektywa Unii Europejskiej nakazująca dużym miastom posiadającym oczyszczalnie badanie ścieków komunalnych pod kątem mikrozanieczyszczeń, w tym także niektórymi antybiotykami, a także bakteriami lekoopornymi i genami lekooporności. Na razie jednak nie ma dokładnej listy, które dokładnie bakterie należy badać. Lista została określona tylko w przypadku antybiotyków. Ma być też wprowadzony dodatkowy stopień oczyszczania, tak aby bakterie lekooporne i pozostałości antybiotyków nie dostawały się do wód gruntowych i powierzchniowych, a tym samym nie przyczyniały się do narastania zjawiska lekooporności.
Źródło: „Gazeta Lekarska” nr 4/2026